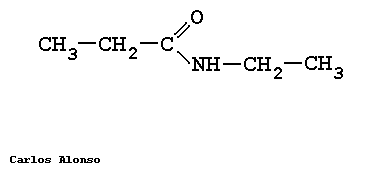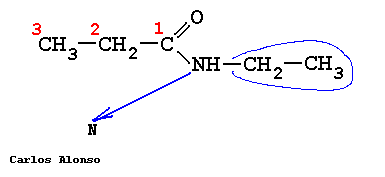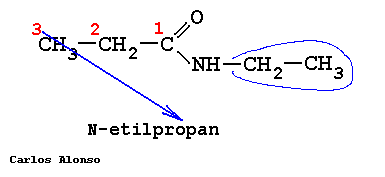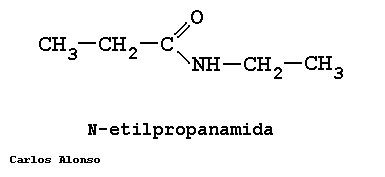
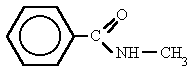
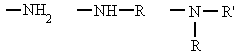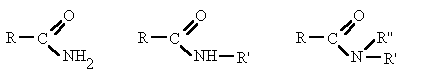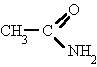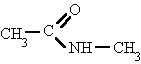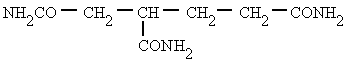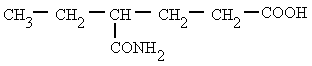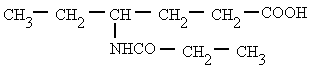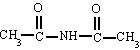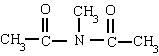Amidas
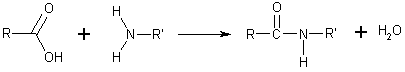
Todas las amidas, excepto la primera de la serie, son sólidas a temperatura ambiente y sus puntos de ebullición son elevados, más altos que los de los ácidos correspondientes. Presentan excelentes propiedades disolventes y son bases muy débiles. Uno de los principales métodos de obtención de estos compuestos consiste en hacer reaccionar el amoníaco (o aminas primarias o secundarias) con ésteres. Las amidas son comunes en la naturaleza, y una de las más conocidas es la urea, una diamida que no contiene hidrocarburos. Las proteínas y los péptidos están formados por amidas. Un ejemplo de poliamida de cadena larga es el nailon. Las amidas también se utilizan mucho en la industria farmacéutica.

Propiedades fisicas
El grupo funcional amida es bastante polar, lo que explica que las amidas primarias, excepto la formamida (p.f.=2,5 ºC), sean todas sólidas y solubles en agua. Sus puntos de ebullición son bastante más altos que los de los ácidos correspondientes, debido a una gran asociación intermolecular a través de enlaces de hidrógeno, entre el oxígeno negativo y los enlaces N—H, mucho más polarizados que en las aminas. Los puntos de fusión y de ebullición de las amidas secundarias son bastante menores, debido principalmente al impedimento estérico del radical unido al nitrógeno para la asociación. Como es natural, las amidas terciarias (sin enlaces N—H) no pueden asociarse, por lo que son líquidos normales, con puntos de fusión y de ebullición de acuerdo con su peso molecular.
Reacciones
Las reacciones químicas de las amidas son las generales de los derivados funcionales de ácidos carboxílicos, si bien son entre éstos, de los compuestos menos reactivos. Así, por ejemplo, la reacción de hidrólisis suele ser muy lenta, por lo que hay que llevarla a cabo calentando y en medios ácidos o básicos; su mecanismo es análogo al de la hidrólisis de los ésteres.
Por otra parte, las amidas tienen también algunas reacciones químicas parecidas a las de las aminas, siendo la más análoga la reacción con ácido nitroso, con el que los tres tipos de amidas se comportan igual que las aminas.
Entre las amidas merece citarse la carbodiamida o urea, que puede considerarse como la diamida del ácido carbónico:
Por otra parte, las amidas tienen también algunas reacciones químicas parecidas a las de las aminas, siendo la más análoga la reacción con ácido nitroso, con el que los tres tipos de amidas se comportan igual que las aminas.
Entre las amidas merece citarse la carbodiamida o urea, que puede considerarse como la diamida del ácido carbónico:
| H2N—O—NH2 |
| urea |
Obtencion
Las amidas pueden obtenerse a partir de halogenuros de alquilo por reacción con amoniaco, aminas primarias o secundarias, con lo que resultan amidas primarias, secundarias o terciarias, respectivamente. Por ejemplo:
| CH3—CO—Cl + | 2 CH3—NH2 | CH3—CO—NH—CH3 + | CH3—NH3+ | Cl- | |
| cloruro de acetilo | metilamina | N-metilacetamida |
Riesgoz
Riesgos
La gran variedad de estructuras químicas posibles de las amidas
se refleja en la diversidad de sus efectos biológicos. Algunas son
completamente inocuas, por ejemplo, las amidas de los ácidos
grasos simples de cadena larga, como las amidas de los ácidos
esteárico u oléico. Por otra parte, algunos miembros de esta
familia han sido clasificados por la Agencia Internacional para la
Investigación sobre el Cáncer (IARC) en el Grupo 2A (probable
carcinógeno humano) o en el Grupo 2B (posible carcinógeno
humano). Con la acrilamida se han observado efectos neuroló-
gicos en el hombre y en animales de experimentación. La dimetilformamida y la dimetilacetamida producen lesiones hepáticas
en los animales y los efectos teratogénicos de la formamida y la
monometilformamida se han demostrado experimentalmente.
Si bien existe una gran cantidad de información acerca del
metabolismo de algunas amidas, la naturaleza de sus efectos
tóxicos aún no se ha explicado a nivel molecular o celular.
Muchas amidas simples son, probablemente, hidrolizadas por la
acción de amidasas inespecíficas en el hígado y el ácido producido se excreta o se metaboliza a través de los mecanismos
normales.
Algunas amidas aromáticas, como la N-fenilacetamida (acetanilida), se hidroxilan en el anillo aromático y, seguidamente, se
conjugan y se excretan. La capacidad de ciertas amidas de penetrar en el organismo a través de la piel intacta es especialmente
importante para la adopción de medidas preventivas
1 Comment